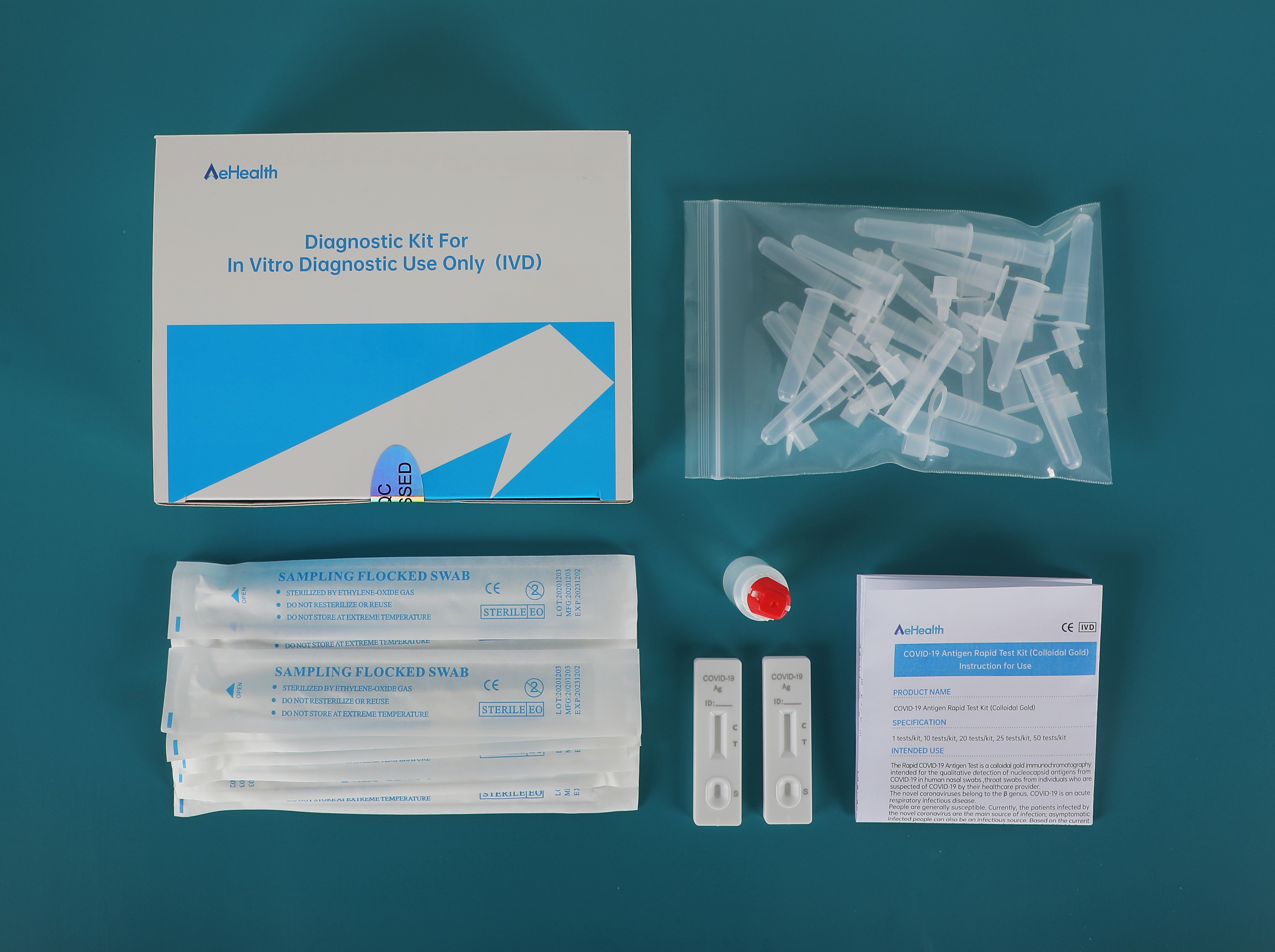
Aehealth는 "인류를 위한 더 나은 의료 서비스"라는 철학을 고수하면서 전 세계적으로 유행하는 전염병을 예방하고 통제하기 위해 신속한 테스트에 대한 글로벌 수요를 충족시키기 위해 지속적으로 노력해 왔습니다.Aehealth 2019-nCoV Antigen Test(colloidal gold )는 비강에서 채취한 면봉 샘플로 수행하며 PCR 방식에 비해 검출 시간이 15분 만에 결과를 제공합니다.테스트는 사용자에게 매우 우수한 품질의 결과로 높은 유연성을 제공할 수 있습니다.
Jens Spahn 독일 보건부 장관은 COVID-19 항원 테스트 승인으로 더 많은 인구가 테스트를 받을 수 있다고 말했습니다.무증상 개인을 조기에 식별하면 감염의 사슬을 효율적으로 끊고 감염 확산을 막을 수 있습니다.
신속 COVID-19 항원 테스트는 의료 제공자가 COVID-19가 의심되는 사람의 비강 면봉, 인후 면봉 또는 타액에서 COVID-19의 뉴클레오캡시드 항원을 정성적으로 검출하기 위한 콜로이드 금 면역크로마토그래피입니다.
신종 코로나바이러스는 β 속에 속한다.COVID-19는 급성 호흡기 감염 질환입니다.
결과는 COVID-19 뉴클레오캡시드 항원을 식별하기 위한 것입니다.항원은 일반적으로 감염의 급성기 동안 상부 호흡기 검체 또는 하부 호흡기 검체에서 검출할 수 있습니다.
양성 결과는 바이러스 항원의 존재를 나타내지만 감염 상태를 결정하기 위해서는 환자 병력 및 기타 진단 정보와의 임상적 상관관계가 필요합니다.
양성 결과는 세균 감염이나 다른 바이러스와의 공동 감염을 배제하지 않습니다.검출된 항원이 질병의 명확한 원인이 아닐 수도 있습니다.
부정적인 결과는 COVID-를 배제하지 않습니다.19 감염이며 감염 통제 결정을 포함하여 치료 또는 환자 관리 결정의 유일한 근거로 사용되어서는 안 됩니다.
음성 결과는 환자의 최근 노출, 병력, COVID-19와 일치하는 임상 징후 및 증상의 존재 맥락에서 고려되어야 하며 환자 관리에 필요한 경우 분자 분석으로 확인되어야 합니다.
Aehealth는 2019-nCoV 항원 테스트 인증서를 보유하고 있는 회사로서 팬데믹과의 글로벌 전투에 기여하기 위해 최선을 다하고 있습니다.Aehealth의 여러 COVID-19 테스트는 CE 마크 승인을 획득했으며 현지 표준 및 규정에 따라 수입국에서 검증되었습니다.애헬스는 현재 코로나19 감염 현장 진단의 다양한 적용 시나리오를 충족하는 'PCR+항원+중화항체' 통합 솔루션을 제공하고 있다.
게시 시간: 2021년 12월 12일